- Allgemeines
- Dosierungen, Darreichungsformen und Anwendungsarten
- Nebenwirkungen, Wechselwirkungen, Kontraindikationen
- Rezeptausstellung
Allgemeines
Patienten mit einer schwerwiegenden Erkrankung und fehlenden Therapiealternativen haben bereits seit März 2017 unter bestimmten Voraussetzungen Anspruch auf eine erstattungsfähige Behandlung mit Medizinalcannabis.
Seit dem 01. April 2024 ist Cannabis durch das „Gesetz zum kontrollierten Umgang mit Cannabis und zur Änderung weiterer Vorschriften“ teilweise legalisiert worden. Es ist u. a. erlaubt, Cannabis privat anzubauen und kleine Mengen getrocknetes Cannabis zum Eigenkonsum zu besitzen, ohne strafrechtlich verfolgt zu werden. Es dürfen bis zu 25 g Cannabis mitgeführt und bis zu 50 g innerhalb der eigenen vier Wände aufbewahrt werden. Gleichzeitig wurde Medizinalcannabis rechtlich klar von Cannabis zu nicht-medizinischen Zwecken (Konsumcannabis) getrennt. Die Regelungen für Medizinalcannabis wurden in ein separates Gesetz (Medizinal-Cannabisgesetz – MedCanG) überführt, wobei die bestehenden Regelungen größtenteils unverändert blieben.
Anspruch auf Versorgung mit Medizinalcannabis
Patienten mit einer schwerwiegenden Erkrankung haben gemäß § 31 Abs. 6 SGB V Anspruch auf eine durch die Gesetzliche Krankenversicherung (GKV) erstattungsfähige Behandlung mit Medizinalcannabis (d. h. mit Cannabis in Form von getrockneten Blüten oder Extrakten in standardisierter Qualität und auf Versorgung mit Arzneimitteln mit den Wirkstoffen Dronabinol oder Nabilon) wenn
1. eine allgemein anerkannte, dem medizinischen Standard entsprechende Leistung
- nicht zur Verfügung steht oder
- im Einzelfall nach der begründeten Einschätzung des Arztes unter Abwägung der zu erwartenden Nebenwirkungen und unter Berücksichtigung des Krankheitszustandes des Patienten nicht angewendet werden kann, und
2. eine nicht ganz entfernt liegende Aussicht auf eine spürbare, positive Einwirkung auf den Krankheitsverlauf oder auf schwerwiegende Symptome besteht.
Wann eine Erkrankung als „schwerwiegend“ definiert wird, hat der G-BA in § 44 Abs. 5 Arzneimittel-Richtlinie konkretisiert: „Eine Krankheit ist schwerwiegend, wenn sie lebensbedrohlich ist oder wenn sie
aufgrund der Schwere der durch sie verursachten Gesundheitsstörung die Lebensqualität auf Dauer nachhaltig beeinträchtigt.“
Hinweis: Die oben genannten Bedingungen sind zwingend erforderlich, um eine Kostenübernahme durch die Krankenkasse zu ermöglichen. Die allgemeine Verordnungsfähigkeit hängt jedoch nicht davon ab, da die Therapieentscheidung im Ermessen des behandelnden Arztes liegt – die Therapiehoheit des Arztes ist gewahrt. Aufgrund der Teillegalisierung unterliegt Cannabis (mit Ausnahme von Nabilon-haltigen Arzneimitteln) auch nicht mehr dem Betäubungsmittelgesetz, wodurch die Einschränkung gemäß § 13 Betäubungsmittelgesetz im Allgemeinen entfällt, wonach Betäubungsmittel nur dann verschrieben werden können, „wenn ihre Anwendung am oder im menschlichen oder tierischen Körper begründet ist. Die Anwendung ist insbesondere dann nicht begründet, wenn der beabsichtigte Zweck auf andere Weise erreicht werden kann.“ Das bedeutet, dass Ärzte Medizinalcannabis verordnen können, auch wenn die Voraussetzungen nach dem SGB V nicht erfüllt sind. Zum Beispiel könnten Ärzte nach einer gründlichen Nutzen-Risiko-Bewertung entscheiden, dass eine Behandlung mit Cannabinoiden anstelle von Biologika besser geeignet ist, z. B. aufgrund eines erhöhten Infektionsrisikos durch diese Arzneimittelgruppe. Ebenso könnte Medizinalcannabis anstelle von Opiaten verschrieben werden, wenn der Arzt das Risiko schwerwiegender Langzeitnebenwirkungen wie etwa Abhängigkeit und Entzugserscheinungen als zu hoch einschätzt.
Verordnungsberechtigung
Zur Verschreibung von Medizinalcannabis sind grundsätzlich alle Personen berechtigt, die zur Ausübung des ärztlichen Berufs befugt sind. Zahnärzte und Tierärzte sind jedoch nicht berechtigt, Medizinalcannabis zu verordnen.
Verordnungsentscheidung
Die Anwendung mit Medizinalcannabis ist im Grunde nie heilend, sondern stets symptomverringernd bzw. -verbessernd. Vor diesem Hintergrund sind Medizinalcannabisverordnungen nicht an eine bestimmte Indikation geknüpft, sondern liegen im Ermessen des behandelnden Arztes.
Mit der Entscheidung über die Therapienotwendigkeit und die Verschreibung von Medizinalcannabis übernimmt somit der behandelnde Arzt grundsätzlich die haftungsrechtliche und wirtschaftliche Verantwortung für die Behandlung.
Hinweis: Bei einer Therapie mit Cannabisarzneimitteln ist die Zweckmäßigkeit einer Weiterbehandlung innerhalb der ersten drei Monate engmaschig und anschließend in regelmäßigen Abständen zu beurteilen. Art, Dauer und Ergebnis des Einsatzes von Medizinalcannabis sind durch den verordnenden Arzt in seiner Patientenakte zu dokumentieren.
Anwendungsgebiete
Die Anwendung von Medizialcannabis kann bei einer Vielzahl von Symptomen und Erkrankungen in Betracht gezogen werden. Generell sollte aber die Anwendung von Medizinalcannabis immer im Rahmen eines therapeutischen Gesamtkonzepts erfolgen und unter Abwägung und Beachtung vorhandener Vor- und Nachteile bzw. zu erwartender Symptombesserung versus potenzieller Risiken und Kontraindikationen.
Mögliche Anwendungsgebiete cannabishaltiger Arzneimittel:
- Chronische/starke Schmerzen (z. B. Phantomschmerzen, Migräne)
- Neurologische Erkrankungen (z. B. Multipler Sklerose, Epilepsie, Tourette-Syndrom)
- Appetitlosigkeit, Erbrechen und schwere Übelkeit (z. B. während einer Chemotherapie, bei HIV- und Aidspatienten oder anderen chronischen Erkrankungen)
- Chronisch entzündliche Erkrankungen (z. B. Rheuma, Morbus Crohn, Colitis Ulcerosa)
- Bestimmte Formen von Epilepsie
- Psychiatrische Erkrankungen (z. B. Depressionen, posttraumatischen Belastungsstörungen oder ADHS)
Gemäß der Begleiterhebung, die vom April 2017 bis März 2022 vom Bundesinstitut für Arzneimittel und Medizinprodukte (BrArM) durchgeführt wurde, waren die häufigsten Anwendungsgebiete:
- Chronische Schmerzsyndrome
- Tumorneubildung
- Spastizität bei Multipler Sklerose (MS)
- Nausea und Erbrechen (z. B. bei Chemotherapie)
- Appetitverlust und Gewichtsabnahme bei HIV/AIDS und Tumorpatienten
Dem Abschlussbericht der Begleiterhebung zufolge verbesserte sich die Symptomatik in fast 75 % der Fälle durch die Anwendung von Medizinalcannabis, während in 70 % der Fälle eine Steigerung der Lebensqualität festgestellt wurde.
Tipp: Es empfiehlt sich, vor jeder Verschreibung von Medizinalcannabis zu prüfen, wie sich die wissenschaftliche Datenlage zu Cannabis und Cannabinoiden in der spezifischen Indikation oder Symptomatik darstellt. Die Studienlage zur medizinischen Anwendung von Cannabis in verschiedenen Indikationsgebieten ist jedoch uneinheitlich. Unter der Rubrik Cannabis-Studien erhalten Sie einen umfassenden Überblick über den aktuellen Stand der Forschung. Eine prägnante Zusammenfassung der wesentlichen Ergebnisse der BfArM-Begleiterhebung finden Sie in der Rubrik Medizinalcannabis. Zudem bietet die Metaanalyse „Cannabinoids for Medical Use: A Systematic Review and Meta-analysis“ eine systematische Übersicht über die Anwendung von Cannabisprodukten. Eine Sammlung strukturierter Kasuistiken (Fallberichte) zur Anwendung von Medizinalcannabis mit detaillierten Daten zu Indikationen, Symptomen, Dosierungen und Nebenwirkungen von Ärzten für Ärzte finden Sie auf der Physicians Experience Platform (PEP, DocCheck-Login erforderlich).
Krankenkasse muss Erstverordnung genehmigen
Die Krankenkasse des Patienten muss die Erstverordnung von Medizinalcannabis genehmigen, bevor dieser mit der Behandlung beginnt. Dies gilt auch für die Verordnung der Fertigarzneimittel (z. B. Sativex® und Canemes®) außerhalb der zugelassenen Indikationen (Off-Label-Use) sowie bei einem grundlegenden Therapiewechsel. Der Antrag auf Genehmigung wird vom Patienten mit Unterstützung des Arztes gestellt. Der Antrag muss gut begründet sein und nachvollziehbar darlegen, dass die notwendigen Voraussetzungen erfüllt sind (siehe auch „Antragstellung zur Kostenübernahme“). Die Krankenkasse kann den Antrag nur in Ausnahmefällen ablehnen.
Ausnahmen von der Genehmigungspflicht
Ausnahmen von der Genehmigungspflicht gelten für Cannabisverordnungen, die im Rahmen der spezialisierten ambulanten Palliativversorgung (SAPV) sowie durch bestimmte Arztgruppen erfolgen. Der Gemeinsame Bundesausschuss (G-BA) hat am 18.07.2024 insgesamt 16 Facharzt- und Schwerpunktbezeichnungen sowie 5 Zusatzbezeichnungen festgelegt, die von der Genehmigungspflicht ausgenommen sind. Der Beschluss trat am 17.10.2024 in Kraft.
Ärzte, die Medizinalcannabis ohne Vorabgenehmigung zulasten der GKV verordnen dürfen:
- Facharzt für Allgemeinmedizin
- Facharzt für Anästhesiologie
- Facharzt für Frauenheilkunde und Geburtshilfe mit Schwerpunkt Gynäkologische Onkologie
- Facharzt für Innere Medizin
- Facharzt für Innere Medizin und Angiologie
- Facharzt für Innere Medizin und Endokrinologie und Diabetologie
- Facharzt für Innere Medizin und Gastroenterologie
- Facharzt für Innere Medizin und Hämatologie und Onkologie
- Facharzt für Innere Medizin und Infektiologie
- Facharzt für Innere Medizin und Kardiologie
- Facharzt für Innere Medizin und Nephrologie
- Facharzt für Innere Medizin und Pneumologie
- Facharzt für Innere Medizin und Rheumatologie
- Facharzt für Neurologie
- Facharzt für Physikalische und Rehabilitative Medizin
- Facharzt für Psychiatrie und Psychotherapie
Auch Ärzte anderer Fachrichtungen können Medizinalcannabis ohne Genehmigung verordnen, wenn sie eine der folgenden Zusatzbezeichnungen erworben haben:
- Zusatzbezeichnung Geriatrie
- Zusatzbezeichnung Medikamentöse Tumortherapie
- Zusatzbezeichnung Palliativmedizin
- Zusatzbezeichnung Schlafmedizin
- Zusatzbezeichnung Spezielle Schmerztherapie
Hinweis: Bei Ärzten, die über diese Facharzt-, Schwerpunkt- oder Zusatzbezeichnung verfügen, geht der G-BA davon aus, dass sie in der Lage sind, die Voraussetzungen für eine Cannabisverordnung umfassend zu beurteilen. Sollten dennoch Unsicherheiten bestehen oder möchten sich die Ärzte vor möglichen finanziellen Rückforderungen (Regresse) absichern – beispielsweise, weil die Krankenkasse die Berechtigung und die Voraussetzungen für die Cannabistherapie anders beurteilen könnte als der behandelnde Arzt oder im Falle einer Folgeverordnung durch weiterbehandelnde Ärzte, wenn die Erstverordnung nicht genehmigt wurde – können auch diese Vertragsärzte selbstverständlich eine (freiwillige) Vorabgenehmigung bei der Krankenkasse beantragen. Es ist jedoch zu beachten, dass eine solche Genehmigung keine abschließende Prüfung darüber beinhaltet, ob eine wirtschaftlichere Auswahl des Cannabisprodukts möglich gewesen wäre.
Bearbeitungsfristen
Die Krankenkassen haben eine Frist von drei Wochen zur Bearbeitung der Anträge, die sich auf fünf Wochen verlängern kann, wenn eine gutachterliche Stellungnahme erforderlich ist. Eine verkürzte Frist von drei Tagen gilt für bestimmte Fälle, wie z. B. Cannabisverordnungen in der allgemeinen ambulanten Palliativversorgung (AAPV) oder bei einer Fortführung einer stationären Cannabistherapie in der ambulanten Versorgung.
Eine erneute Genehmigung ist nicht erforderlich für Folgeverordnungen, bei einem Arztwechsel, Dosisanpassungen oder einem Wechsel innerhalb der Blüten oder Extrakte in standardisierter Form.
Hinweis: Die Kostenübernahme durch die Krankenkassen ist keine zwingende Bedingung für die Verordnung. Patienten können Medizinalcannabis – sofern medizinisch indiziert und begründet – auch auf eigene Kosten erhalten (Privatverordnung).
Fertigarzneimittel vor Blüten und Extrakte
Medizinalcannabis kann in Form von Fertigarzneimitteln wie Sprays, Lösungen oder Kapseln und als Rezepturarzneimittel in Form von Cannabisblüten bzw. -extrakten sowie Dronabinolzubereitungen verschrieben werden.
Vor der Verschreibung von getrockneten Cannabisblüten oder -extrakten sollten Ärzte prüfen, ob geeignete cannabishaltige Fertigarzneimittel für die Behandlung des jeweiligen Patienten verfügbar sind. Grundsätzlich weisen Fertigarzneimittel und standardisierte Extrakte besser definierte pharmakologische Eigenschaften auf. Die Verordnung von Cannabisblüten sollte begründet werden. Dabei ist, wie bei anderen Verordnungen auch, das Wirtschaftlichkeitsgebot zu beachten.
Rezepturzubereitungen
Folgende standardisierte Rezepturvorschriften stehen seitens der DAC/NRF-Kommission (Deutscher Arzneimittel-Codex/Neues Rezeptur-Formularium) zur Verfügung:
- Dronabinol-Kapseln zu 2,5 bzw. 5 oder 10 mg (NRF 22.7.)
- Dronabinol-Tropfen 25 mg/ml (2,5-%ige) ölige Lösung (NRF 22.8.)
- Ölige Cannabidiol-Lösung 50 mg/ml; 100 mg/ml; 200mg/ml; 400 mg/ml (NRF 22.10.)
- Ölige Cannabisölharz-Lösung 25 mg/ml Dronabinol (NRF 22.11.)*
- Cannabisblüten zur Inhalation nach Verdampfung (NRF 22.12.)
- Cannabisblüten in Einzeldosen zur Inhalation nach Verdampfung (NRF 22.13.)
- Cannabisblüten zur Teezubereitung (NRF 22.14.)
- Cannabisblüten in Einzeldosen zu 0,25 g; 0,5 g; 0,75 g oder 1 g zur Teezubereitung (NRF 22.15.)
- Ethanolische Dronabinol-Lösung 10 mg/ml zur Inhalation (NRF 22.16.)
- Cannabidiol-Kapseln 10 bis 250 mg (NRF 22.17.)
* Zurzeit nicht praktikabel, da das für die Rezeptur benötigte eingestellte, raffinierte Cannabisölharz aktuell nicht hergestellt wird.
Ärzte können sich im DAC/NRF über die Rezepturvorschriften informieren (Zugang mit DocCheck-LogIn). Zu jeder Rezepturvorschrift gibt es auch einen Link zu einer Musterverordnung.
Verordnungsfähigkeit nicht zugelassener Cannabisarzneimittel
Ob der gesetzliche Anspruch von Patienten auf eine Versorgung mit Medizinalcannabis auch eine Verordnung von in Deutschland nicht zugelassenen Cannabisarzneimittel begründet, lässt sich derzeit nicht abschließend bewerten. Einzelimporte von in Deutschland nicht zugelassenen Arzneimitteln (z. B. Marinol® Kapseln oder Syndros® Orallösung aus den USA) werden bislang in nur sehr eng definierten Einzelfällen von der Gesetzlichen Krankenversicherung (GKV) übernommen. Im konkreten Einzelfall ist daher eine Vorabklärung mit der jeweiligen Krankenkasse anzuraten (über den Patienten mittels Genehmigungsantrag).
Folgende Punkte müssen für die rechtliche Zulässigkeit eines Einzelimports nach § 73 Abs. 3 Arzneimittelgesetz (AMG) u. a. erfüllt sein:
- Bestellung in geringer Menge für eine einzelne Person
- Arzneimittel ist in dem Staat, aus dem es nach Deutschland importiert wird, rechtmäßig in Verkehr
- Keine hinsichtlich des Wirkstoffs identischen und hinsichtlich der Wirkstärke vergleichbaren Arzneimittel für das betreffende Anwendungsgebiet in Deutschland verfügbar
- Keine Rücknahme, kein Widerruf, kein Ruhen der Zulassung in Deutschland gem. § 30 Abs. 4 AMG
- Keine Dopingsperre
- TSE-Verordnung zutreffend und erfüllt
- § 5 (Verbot bedenklicher Arzneimittel) und § 8 (Verbote zum Schutz vor Täuschung) AMG sind nicht betroffen
Dosierungen, Darreichungsformen und Anwendungsarten
Dosierungen
Standardisierte Dosierungsschemata gibt es für die Anwendung von Medizinalcannabis nicht. Die Dosierung erfolgt individuell für jeden Patienten und hängt unter anderem von der Art der Erkrankung, dem Schweregrad der Symptome, der Anwendungsart sowie von individuell auftretenden unerwünschten Arzneimittelwirkungen (UAW) bzw. Nebenwirkungen ab.
Grundsätzlich gilt das Prinzip „Start low, go slow, keep low but treat to target“. Das bedeutet, dass die Therapie, unabhängig vom Produkt, stets mit einer sehr geringen Anfangsdosis beginnen und langsam gesteigert werden sollte, beispielsweise alle 1–3 Tage um eine Einheit, bis die gewünschten Wirkungen oder Symptombesserungen eintreten. Wenn Nebenwirkungen auftreten, wie zum Beispiel Schwindel, sollte die Dosierung wieder um eine Einheit reduziert werden.
Folgende Dosierempfehlungen – gemäß der Bundesärztekammer und dem Handbuch „Cannabis: Verordnungshilfe für Ärzte“ von Grotenhermen/Häußermann – können als Ansatzpunkte dienen.
Cannabisblüten:
Medizinalcannabisblüten sind ein Naturprodukt, dessen Inhaltsstoffkonzentrationen von Blüte zu Blüte variieren können, beispielsweise abhängig von der Genetik der Mutterpflanze. Der Gesetzgeber gestattet Importeuren und Herstellern gewisse Schwankungen der Werte und erteilt Sondergenehmigungen für leichte Abweichungen einzelner Chargen. Es ist jedoch nicht verpflichtend für die Importeure, die spezifischen Varietäten offenzulegen, was dazu führen kann, dass unter denselben Sortennamen unterschiedliche Genetiken existieren.
Tipp: Um eine sichere und präzise Dosierung zu gewährleisten, empfiehlt es sich, beim Apotheker nach möglichen Änderungen in der Zusammensetzung einzelner Sorten zu fragen.
- Anfangsdosis bei höherem THC-Gehalt (> 10 %): 25–50 mg Cannabisblüten pro Tag (per Inhalation)
- Anfangsdosis bei geringem THC-Gehalt: max. 100 mg Cannabisblüten pro Tag (per Inhalation)
Mit Blick auf Wirksamkeit und Verträglichkeit sollte die Dosis alle ein bis drei Tage um 2,5–5 mg THC gesteigert werden (entspricht je nach Sorte ca. 25–100 mg Cannabis-Blüten).
Nach bisherigen Erfahrungen liegen die Tagesdosen THC-reicher Cannabissorten meist bei 0,1–3 g (Schwankungen von 0,05–10 g möglich).
Hinweis: Aufgrund der unterschiedlichen Wirkstoffkonzentration in einzelnen Blütenteilen empfiehlt die Bundesapothekerkammer (BAK), Cannabisblüten – zum Zweck der Dosiergenauigkeit – vor der Abgabe an Patienten, durch Apotheken zerkleinern und sieben zu lassen.
Cannabisextrakte:
- Anfangsdosis: 1–2,5 mg THC (+ 1–5 mg CBD) pro Tag (orale Einnahme)
- Tagesdosis: max. 40 mg THC mit CBD-Zusatz (orale Einnahme)
Die Anwendungshäufigkeit ist individuell und variiert von 1-mal bis mehrmals täglich.
Dosissteigerungen sollten möglichst mit der abendlichen Einnahme erfolgen (Verlegung möglicher UAW in die Schlafenszeit).
Dronabinol:
- Anfangsdosis: 1–2 x 2,5 mg THC pro Tag (orale Einnahme)
- Tagesdosis: bis 30 mg ohne CBD-Zusatz (orale Einnahme)
Cannabidiol:
- Anfangsdosis: 2 x 2,5 mg/kg Körpergewicht pro Tag (orale Einnahme)
- Tagesdosis: max. 20 mg/kg Körpergewicht (orale Einnahme)
Fertigarzneimittel:
Bezüglich der Fertigarzneimittel Sativex®, Canemes® und Epidyolex® sowie der Importarzneimittel Marinol® und Syndros® verweisen wir auf die jeweiligen Fachinformationen.
>> Zur Fachinformation Sativex®
>> Zur Fachinformation Canemes®
>> Zur Fachinformation Epidyolex®
>> Zur Fachinformation Marinol®
>> Zur Fachinformation Syndros®
Darreichungsformen und Anwendungsarten
Medizinalcannabis kann inhaliert oder auch oral aufgenommen werden. Im Vergleich zur inhalativen Anwendung ist die Bioverfügbarkeit bei oraler Anwendung geringer. Die geeignete Einnahmeform hängt unter anderem von der Indikation, der körperlichen Verfassung des Patienten, gegebenenfalls von Begleiterkrankungen und auch vom Wunsch des Patienten ab. In einigen Fällen kann auch eine Kombination aus inhalativer und oraler Einnahmeform sinnvoll sein.
Wirkeintritt und Wirkdauer
Durch Inhalation verabreichte Cannabisblüten verfügen über einen schnellen Wirkeintritt. Bereits nach 3–10 Minuten kann es zu einer Symptomlinderung kommen, die ca. 2–4 Stunden anhält. Blüten eignen sich somit z. B. gut für eine Akuttherapie.
Bei oral eingenommenen Cannabisextrakten und Dronabinol-Präparate dauert es 1–3 Stunden, bis es zu einem Wirkeintritt kommt. Die Symptomlinderung kann bis zu 6 oder 8 Stunden anhalten. Der Wirkeintritt ist auch vom Füllgrad des Magens abhängig: Je voller dieser ist, desto langsamer tritt eine Symptomlinderung ein. Ob die Einnahme vor oder nach dem Essen erfolgt, ist nicht von Bedeutung. Der Patient sollte darauf achten, das Arzneimittel jeweils zum gleichen Zeitpunkt einzunehmen, um Schwankungen beim Wirkeintritt zu vermeiden und somit die individuelle Dosiseinstellung zu erleichtern.
Bei der Ersteinstellung von Cannabis-unerfahrenen Patienten werden zudem leichter dosierbare und individuell gut titrierbare Darreichungsformen empfohlen, wie z. B. Dronabinol-Tropfen oder Sativex® Mundspray.
Hinweis: Da die Darreichungsform und Anwendungsart meist auch vom ausgewählten Cannabisprodukt abhängt, ist mit der Entscheidung für ein bestimmtes Produkt auch die Wirtschaftlichkeit der Verordnung betroffen. Die Cannabisverordnung ist damit auch immer eine Behandlungsoption, über die der Arzt unter Berücksichtigung der Notwendigkeit, Zweckmäßigkeit und Wirtschaftlichkeit zu entscheiden hat. Die Therapieentscheidung sollte immer sorgfältig und nachvollziehbar in der Patientenakte dokumentiert werden.
Inhalative Anwendung
Cannabisblüten können inhalativ über die Verwendung eines Verdampfers/Vaporisators erfolgen. Dabei werden die Cannabisblüten über 185 °C erhitzt, sodass die Cannabinoide frei werden. Es bildet sich ein inhalierbares Aerosol. Bei der Inhalation flutet die Plasmakonzentration sehr schnell an (Maximum nach 3–10 Minuten) und sinkt ebenso schnell wieder ab. Auch Dronabinol kann als ethanolische Lösung zur Inhalation zubereitet werden. Cannabisextrakte werden wiederum oral eingenommen, da sich beim Erhitzen gesundheitsschädliche Pyrolyseprodukte aus der öligen Trägersubstanz bilden können.
Folgende Vaporisatoren sind zulasten der GKV auf einem zusätzlichen Muster-16-Rezept verordnungsfähig (ab 01.07.2027 als E-Rezept):
- Volcano Medic 2 (PZN: 15885501): Tisch-Vaporisator, der sich mit einem Ventilballon oder Schlauch verwenden lässt. Bei der Verwendung des Ballons, muss der Inhalt innerhalb von 10 Minuten nach Befüllung inhaliert werden. Geeignet zur Verdampfung von getrockneten Cannabisblüten und auch Dronabinol.
- Mighty + Medic (PZN: 16616803): Tragbarer Vaporisator, der eine Inhalation auch unterwegs ermöglicht. Nur zur Verneblung von getrockneten Cannabisblüten geeignet.
Vaporisatoren sind bislang nicht im Hilfsmittelverzeichnis gelistet. Deshalb ist eine Vorabgenehmigung der Kostenübernahme für Patienten bei der jeweiligen Krankenkasse erforderlich.
Hinweis: Im Gegensatz zu Arzneimittelverordnungen muss für eine korrekt ausgefüllte Verordnung eines Hilfsmittels – gemäß § 7 Abs. 2 Hilfsmittel-Richtlinie – immer die Diagnose auf dem Rezept (z. B. verschlüsselt als ICD-Code) genannt werden.
Orale Anwendung
Cannabishaltige Fertigarzneimittel sowie das Rezepturarzneimittel Dronabinol werden in der Regel oral aufgenommen, entweder als Spray, als Kapsel oder im Fall von Dronabinol auch in Tropfenform. Die Aufnahme nach peroraler Applikation ist langsam und individuell sehr unterschiedlich. Maximale Plasmaspiegel treten nach 1–6 Stunden auf.
Grundsätzlich kann eine orale Einnahme vor oder auch nach einer Mahlzeit erfolgen. In der Einstellungsphase sollten Patienten allerdings nicht zwischen den Einnahmezeitpunkten wechseln, da die Nahrung den Wirkungseintritt beeinflussen kann.
Cannabis rauchen, Tee- und Kekszubereitung
Grundsätzlich ist das Rauchen von getrockneten Cannabisblüten (zusammen mit Tabak) möglich, aber aus gesundheitlichen Gründen nicht empfehlenswert, da beim Rauchen schädliche Verbrennungsprodukte entstehen. Daher ist für eine inhalative Anwendung die Inhalation mittels Vaporisator zu bevorzugen.
Eine weitere Option besteht in der Teezubereitung. Diese ist jedoch aufwendiger und anfällig für potenzielle Fehler. Bei der Herstellung der Teezubereitung handelt es sich um einen standardmäßigen Ansatz von 0,5 g Droge auf 0,5 l Wasser, das über 15 Minuten sieden muss. Die Ausbeute an THC beträgt etwa 10 mg/l. Dies erklärt sich durch die begrenzte Wasserlöslichkeit der Cannabinoide und die bei 100 °C nur langsam verlaufenden Decarboxylierungsreaktionen. Aus diesem Grund sollte Medizinalcannabis möglichst nicht als Tee zubereitet und eingenommen werden. Soll die Anwendung dennoch als Teezubereitung erfolgen, dann ist die Tasse Tee am besten warm zu trinken und etwas Sahne hinzuzufügen, damit sich die lipophilen Cannabinoide besser im Getränk lösen. Die Ausbeute lässt sich zudem durch eine längere Kochzeit vergrößern, bei 30 Minuten erhöht sie sich um ca. das Eineinhalbfache.
Auch das Einbacken in Keksteig kann aus Gründen der Arzneimitteltherapiesicherheit nicht empfohlen werden, denn die Dosis pro Anwendung kann nicht sicher reproduziert werden.
Nebenwirkungen, Wechselwirkungen, Kontraindikationen
Nebenwirkungen
Insbesondere zu Therapiebeginn können Nebenwirkungen auftreten, die bei Frauen in der Regel häufiger auftreten als bei Männern. In den meisten Fällen handelt es sich um Schwindel, Benommenheit bzw. Müdigkeit, Mundtrockenheit, Konzentrations- und Gedächtnisstörungen, Übelkeit und/oder Durchfall. Sollte der Patient eine oder mehrere dieser Nebenwirkungen bei sich feststellen, kann eine Anpassung der Dosierung und/oder Darreichungsform Abhilfe schaffen. Gegebenenfalls kann auch ein Wechsel zu einem Präparat mit einem anderen THC- und/oder CBD-Gehalt erforderlich sein. Diese Nebenwirkungen müssen jedoch nicht zwangsläufig zu einem Abbruch der Therapie führen.
Weitere mögliche Nebenwirkungen sind unter anderem Stimmungsänderungen (Euphorie, „High“-Gefühl, Dysphorie), Steigerung des Appetits, Muskelrelaxation, Tachykardie, orthostatische Hypotension und kardiale Ischämie, in Einzelfällen bis zum Myokardinfarkt.
Hinweis: Insbesondere Cannabisblüten mit einem hohen THC-Gehalt bergen ein Risiko für psychotische Ereignisse, selbst bei regelmäßigen Konsumenten. Darüber hinaus besteht ein nicht zu vernachlässigendes allergenes Potenzial und Risiken für Wechselwirkungen mit anderen Arzneimitteln.
Weitere Informationen zu Nebenwirkungen im Rahmen einer Behandlung mit Medizinalcannabis können beispielsweise der Studie „General risks of harm with cannabinoids, cannabis, and cannabis-based medicine possibly relevant to patients receiving these for pain management: an overview of systematic reviews“ entnommen werden.
Wechselwirkungen
Da es sich bei Cannabis um ein Polywirkstoffgemisch handelt und nicht um einen chemisch definierten Einzelwirkstoff, sind die möglichen Wechselwirkungen mit anderen Arzneimitteln, Lebensmitteln und Genussmitteln vielfältig. Medizinalcannabis kann beispielsweise zu einem Wirkungsverlust, einer Wirkungsverstärkung oder auch zu Überdosierungen führen.
Pharmakokinetische und pharmakodynamische Interaktionen
Wechselwirkungen können sich auf pharmakokinetische oder pharmakodynamischer Ebene abspielen. Zu den pharmakokinetischen Interaktionen zählt z. B. die sehr hohe Plasma-Protein-Bindung (PPB) von THC von 95–99 %, d. h. THC kann andere Substanzen aus deren Bindung leicht verdrängen. Folglich stehen diese Substanzen den Zielgeweben in einer höheren Menge in freier Form zur Verfügung und es kommt zu einer Wirkungsverstärkung der verdrängten Substanzen.
Weitere pharmakokinetische Wechselwirkungen sind die Hemmung oder Induktion metabolischer Enzyme, wie z. B. des Cytochrom-P450-(CYP)Systems in der Leber, welches für den Um- bzw. Abbau zahlreicher Wirkstoffe verantwortlich ist. THC, CBD und CBN hemmen unter anderem CYP3A4, CYP2D6 und CYP2C9. Die Wirkung von z. B. Antidepressiva, Antimykotika, Chemotherapeutika, Immunsuppressiva und Vitamin-K-Antagonisten (Phenprocoumon) können daher, bei gleichzeitiger Anwendung mit Medizinalcannabis, ansteigen. Verhindert das durch Cannabis gehemmte CYP-Enzym wiederum die Umwandlung eines Prodrugs (z. B. Clopidogrel) in seinen aktiven Metaboliten, kann es zu einer Wirkungsminderung des gleichzeitig eingenommenen Arzneimittels kommen.
Aber auch der gegenteilige Effekt ist möglich: Gleichzeitig eingenommene Arzneimittel beeinflussen die Wirkung des Medizinalcannabis. Da auch THC und CBD über hepatische CYP-Enzyme abgebaut werden, können bestimmte CYP3A4- und/oder CYP2C9-Inhibitoren den Abbau von THC bzw. CBD und deren Metaboliten verlangsamen und somit die cannabinoiden Effekte verstärken. Das betrifft z. B. CYP3A4-Inhibitoren wie Ketoconazol, Itraconazol, Makrolidantibiotika, Ritonavir oder Verapamil bzw. CYP2C9-Inhibitoren wie Amiodaron, Cotrimoxazol, Fluconazol oder Fluoxetin.
Medizinalcannabis interagiert auch mit mehreren Transportproteinen, u. a. hemmen Cannabinoide den Transporter P-Glykoprotein (Pgp). Werden andere Substrate von Pgp gleichzeitig mit Cannabis eingenommen, können diese somit eine erhöhte Bioverfügbarkeit bzw. Wirksamkeit aufweisen. Dies betrifft z. B. direkte orale Antikoagulanzien (DOAK) wie Apixaban, Dabigatran und Rivaroxaban.
Beispiele für pharmakodynamische Interaktionen sind die Verstärkung der Müdigkeit und Herabsetzung der Reaktionsfähigkeit bei gleichzeitiger Gabe von psychotrop wirkenden Stoffen, wie z. B. Benzodiazepinen oder Alkohol, eine Herabsetzung des Muskeltonus und -kraft und somit eine erhöhte Sturzgefahr bei gleichzeitiger Anwendung von Antispastika oder die Muskelrelaxierung in Verbindung mit Hypnotika und Sedativa.
Hinweis: Welche dieser Interaktionen eine reale klinische Relevanz aufweisen, lässt sich derzeit – aufgrund der aktuell noch mageren Studienlage – nur spekulieren. Die Webseite www.drugs.com verzeichnet aber derzeit insgesamt 399 Wechselwirkungen im Zusammenhang mit Cannabis. Davon sind 28 als schwerwiegend und 371 als moderat eingestuft, die bei der Überprüfung von Interaktionen aktuell berücksichtigt werden sollten.
Kontraindikationen
- Hypersensitivtätsreaktionen gegenüber Medizinalcannabis
- Schwangerschaft und Stillzeit
- Schwere Persönlichkeitsstörungen oder psychotische Erkrankungen
Strenge Indikationsstellung
- Schwere Herz-Kreislauf-Erkrankungen
- Hepatitis C
- Suchterkrankungen
- Krampfanfälle in der Anamnese
- Kinder und Jugendliche bis 18 Jahren
- Ältere Patienten, aufgrund einer per se gesteigerten Anfälligkeit für zentralnervöse und kardiovaskuläre Komplikationen
- Niedrigere Startdosis bei Patienten mit Leber- oder Niereninsuffizienz
- Intensive Überwachung während einer perioperativen Phase
Rezeptausstellung
Die Verschreibung von Medizinalcannabis erfolgt seit dem 01. April 2024 grundsätzlich auf einem E-Rezept. Aufgrund von technischen Schwierigkeiten bei der Umsetzung kann jedoch auch ein papiergebundenes Muster-16-Rezept oder, in Einzelfällen, ein Betäubungsmittel(BtM)-Rezept verwendet werden (solche Cannabis-BtM-Rezepte haben eine Gültigkeit von 28 Tagen). §§ 2 und 4 der Arzneimittelverschreibungsverordnung (AMVV) gelten entsprechend. Synthetische Cannabinoide der Anlage III Betäubungsmittelgesetz (Nabilon-haltige Arzneimittel) müssen weiterhin auf einem BtM-Rezept (ab 01.07.2025 als E-Rezept) verordnet werden.
Das E-Rezept
Welche Angaben auf einer Arzneimittelverordnung gemacht werden müssen, ist in § 2 der Arzneimittlverschreibungverordnung (AMVV) geregelt.
Demnach sind auf einem E-Rezept (bzw. Muster-16-Rezept) für getrocknete Cannabisblüten, Cannabisextrakte sowie cannabishaltige Arzneimittel u. a. folgende Angaben notwendig:
- Name, Vorname, Berufsbezeichnung und Anschrift der Praxis oder der Klinik der verschreibenden ärztlichen Person einschließlich einer Telefonnummer zur Kontaktaufnahme
- Datum der Ausfertigung oder, bei Verschreibungen in elektronischer Form, das Datum der qualifizierten elektronischen Signatur
- Name und Geburtsdatum der Person, für die das Arzneimittel bestimmt ist
- Bezeichnung des Fertigarzneimittels oder des Wirkstoffes einschließlich der Stärke; bei einem Arzneimittel, das in der Apotheke hergestellt werden soll, die Zusammensetzung nach Art und Menge oder die Bezeichnung des Fertigarzneimittels, von dem eine Teilmenge abgegeben werden soll, sowie eine Gebrauchsanweisung; z. B. ölige Dronabinol-Tropfen 25 mg/ml (NRF 22.8) 10 ml (entspricht 250 mg Dronabinol)]; bei Cannabisblüten und Cannabisextrakten muss explizit auch die Sorte bzw. der Extrakt genannt werden (am besten auch Hersteller und PZN), da sich die Sorten/Extrakte in ihrem Wirkstoffgehalt unterscheiden. Eine reine Wirkstoffverordnung unter Angabe z. B. des THC-Gehalts ist nicht zulässig.
- Darreichungsform, sofern dazu die Bezeichnung nach Nummer 4 nicht eindeutig ist
- Abzugebende Menge des verschriebenen Arzneimittels; sofern das Arzneimittel zur wiederholten Abgabe auf dieselbe Verschreibung bestimmt sein soll, einen Vermerk mit der Anzahl der Wiederholungen
- Dosierung; dies gilt nicht, wenn dem Patienten ein Medikationsplan, der das verschriebene Arzneimittel umfasst, oder eine entsprechende schriftliche Dosierungsanweisung einer verschreibenden Person vorliegt und wenn die verschreibende Person dies in der Verschreibung kenntlich gemacht hat oder wenn das verschriebene Arzneimittel unmittelbar an die verschreibende Person abgegeben wird. Spezialfall Rezepturverordnung: Bei einem Arzneimittel, das in der Apotheke hergestellt werden soll, muss eine Gebrauchsanweisung zusätzlich angegeben werden (einer Gebrauchsanweisung bedarf es nicht, wenn das Arzneimittel unmittelbar an die verschreibende Person abgegeben wird); ist sie nur mit dem Hinweis „Gemäß schriftlicher Anweisung“ gekennzeichnet, so muss die Anweisung der Apotheke zusätzlich in schriftlicher Form vorliegen (nach ärztlicher Rücksprache darf die Apotheke diese auf dem Rezept ergänzen). Grund ist die Kennzeichnungspflicht der Primärverpackung eines Rezepturarzneimittels nach § 14 Apothekenbetriebsordnung (ApBetrO). Ist die schriftliche Anweisung der Apotheke nicht bekannt, so ist die Verordnung nicht plausibel und die Rezeptur darf – bis zur Klärung – nicht hergestellt werden.
- Gültigkeitsdauer der Verschreibung
- Eigenhändige Unterschrift der verschreibenden Person oder, bei Verschreibungen in elektronischer Form, deren qualifizierte elektronische Signatur
Rezeptbeispiele (Ausschnitt):

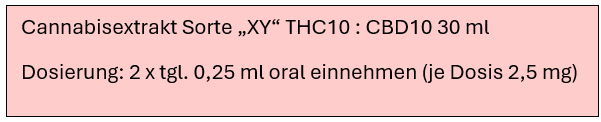
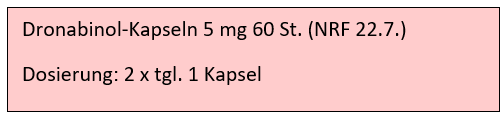
Das BtM-Rezept (Nabilon-haltige Arzneimittel)
Ein BtM-Rezept besteht immer aus drei Teilen: einem gelben Deckblatt (Teil II) und zwei Durchschlägen (Teil I und III). Teil III verbleibt zur Dokumentation in der Arztpraxis des verordnenden Arztes, während Teil I und II in der Apotheke vorgelegt werden.
Nach § 9 der Betäubungsmittel-Verschreibungsverordnung (BtMVV) sind auf einem Betäubungsmittelrezept (z. B. für Nabilon-haltige Arzneimittel) u. a. folgende Angaben notwendig:
- Name, Vorname und Anschrift des Patienten
- Ausstellungsdatum
- Arzneimittelbezeichnung, soweit dadurch eine der nachstehenden Angaben nicht eindeutig bestimmt ist, jeweils zusätzlich Bezeichnung und Gewichtsmenge des enthaltenen Betäubungsmittels je Packungseinheit, bei abgeteilten Zubereitungen je abgeteilter Form, Darreichungsform
- Menge des verordneten Arzneimittels in Gramm oder Milliliter, Stückzahl der abgeteilten Form
- Gebrauchsanweisung/Dosierungsangabe mit Einzel- und Tagesgabe: Ist das Rezept nur mit dem Hinweis „Gemäß schriftlicher Anweisung“ gekennzeichnet, so muss die Anweisung der Apotheke zusätzlich in schriftlicher Form vorliegen. Grund ist die Kennzeichnungspflicht der Primärverpackung eines Rezepturarzneimittels nach § 14 Apothekenbetriebsordnung (ApBetrO). Ist die schriftliche Anweisung der Apotheke nicht bekannt, so ist die Verordnung nicht plausibel und die Rezeptur darf – bis zur Klärung – nicht hergestellt werden.
- Name des verschreibenden Arztes, Berufsbezeichnung, Anschrift und Telefonnummer sowie Unterschrift
- Betriebsstättennummer (BSNR) und lebenslange Arztnummer (LANR)
- Seriennummer: Jeder Rezeptvordruck hat eine einmalige, neunstellige Seriennummer. Diese ist mit einer schwarzen Farbe aufgedruckt, die unter UV-A-Licht grünlich fluoresziert
Hinweis: In der Betäubungsmittelverschreibungsverordnung (BtMVV) waren Höchstmengen definiert, die ein Arzt höchstens für einen Zeitraum von 30 Tagen für einen Patienten verordnen durfte. Bei Überschreitung der vorgegebenen Höchstmenge musste der Arzt dies durch den Buchstaben „A“ auf dem BtM-Rezept kenntlich machen. Die Höchstmengenregelung und die Kennzeichnungspflicht bei Überschreitung sind seit dem 08.04.2023 nicht mehr gültig.
Rezeptbeispiel (Ausschnitt):

Auf folgende Besonderheiten bei der Rezeptausstellung achten:
- Die Verordnung mehrerer Cannabisprodukte (z. B. zwei Cannabisblütensorten) ist grundsätzlich möglich, sollte aber auf getrennten Rezepten erfolgen. Laut „Erläuterungen zur Anlage 2 – Vereinbarung über Vordrucke für die vertragsärztliche Versorgung“ zum Bundesmantelvertrag (BMV) der Ärzte (gültig ab 01. Juli 2024) darf grundsätzlich nur die Vorderseite des Vordrucks benutzt werden. Pro Rezeptur ist daher ein Verordnungsblatt (Muster-16-Papierrezept) zu verwenden. Hinweis: Wenn Medizinalcannabis auf einem E-Rezept verordnet wird, können theoretisch auch mehrere Rezepturen auf einem Rezept verordnet werden, da die Bedruckung mit dem Hash-Code bei E-Rezepten wegfällt.
- Bei der Verordnung einer Rezeptur ist der alleinige Hinweis („Dj“, „nach schriftlicher Anweisung“ oder der Wert „false“ bei E-Rezepten) nicht ausreichend, da die Apotheke die Gebrauchsanweisung auf Plausibilität prüfen und auf dem Abgabegefäß angeben muss. Wird dennoch „gemäß schriftlicher Anweisung“ verordnet, muss diese der Apotheke unbedingt bekannt sein. Ist diese unbekannt, muss die Verordnung als „nicht plausibel“ gewertet werden und das Rezepturarzneimittel darf nicht hergestellt werden, bis der Sachverhalt geklärt ist. Es empfiehlt sich daher, die Gebrauchsanweisung stets eindeutig definiert auf dem Rezept zu vermerken.
- Wie bei allen anderen Arzneimittelverordnung, darf auf dem Rezept keine Diagnose oder Therapiebegründung angegeben werden. Eine Diagnose ist aber für eine korrekt ausgefüllte Verordnung eines Hilfsmittels (z. B. Vaporisator) gemäß § 7 Abs. 2 Hilfsmittel-Richtlinie erforderlich.
- Arzneimittel sollen nicht gemeinsam mit einem Hilfsmittel auf demselben Rezept verordnet werden (keine „Mischverordnungen“).